Ammoniac
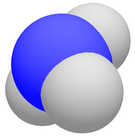
L'ammoniac est un composé chimique, de formule NH 3 et dégageant une odeur très forte et désagréable. C'est une molécule pyramidale trigonale : l'azote (N) est au centre alors que l'hydrogène (H) occupe trois des quatre sommets, le quatrième...
Définitions :
- Relatif à l'ammoniac; Composé chimique de formule NH3. Une molécule d'ammoniac est composée d'un atome d'azote et de trois atomes d'hydrogène (source : fr.wiktionary)
- Gaz incolore formé d'un atome d´azote et de trois atomes d'hydrogène. Il est fortement alcalin en solution aqueuse. (source : biofondations.gc)
|
|||||
|---|---|---|---|---|---|
|
|
|||||
| Général | |||||
| Formule brute | NH3 | ||||
| Nom IUPAC | ammoniac | ||||
| Numéro CAS | 7664-41-7 | ||||
| Apparence | Gaz incolore | ||||
| Propriétés physiques | |||||
| Masse moléculaire | 17,03056 | ||||
| Température de fusion |
195,45 K (-77,7 °C) | ||||
| Température de vaporisation |
239,8 K (-33,35 °C) | ||||
| Solubilité | 90 g dans 100g d'eau à 0°C | ||||
| Densité | 0,6813 (gaz) | ||||
| Température d'auto-inflammation |
651°C | ||||
| Limites d'explosivité dans l'air |
Inférieure : 15,5 (Weiss, 1985) Supérieure : 27 (Weiss, 1985) |
||||
| Thermochimie | |||||
| S0gaz, 1 bar | 192,77 J/mol·K | ||||
| S0liquide, 1 bar | ? J/mol·K | ||||
| S0solid | ? J/mol·K | ||||
| ΔfH0gaz | -45,9 kJ/mol | ||||
| ΔfH0liquide | -40,2 kJ/mol | ||||
| ΔfH0solide | ? kJ/mol | ||||
| Toxicologie | |||||
| Inhalation | Les vapeurs sont très irritantes et corrosives |
||||
| Peau | Les solutions concentrées peuvent provoquer des brûlures |
||||
| Yeux | Dangereux | ||||
| Ingestion | L'ingestion peut provoquer des brûlures de la bouche, langue, œsophage |
||||
| Unités du SI & CNTP, sauf indication contraire. |
|||||
L'ammoniac est un composé chimique, de formule NH3 et dégageant une odeur très forte et désagréable. C'est une molécule pyramidale trigonale : l'azote (N) est au centre alors que l'hydrogène (H) occupe trois des quatre sommets, le quatrième étant occupé par 2 électrons.
Propriétés
- Odeur : très âcre et aisément reconnaissable, irrespirable (mortel pour l'homme).
- Inflammabilité et explosibilité : Sous forte pression le R717 peut former un mélange explosif avec les huiles de lubrification mais aussi le mélange air-ammoniac s'enflamme et explose violemment.
- Surchauffe de compression : La valeur élevée du rapport α=Cp/Cv = 1,335 à 0°C limite rapidement le taux de compression acceptable du fait des hautes températures des vapeurs de refoulement, températures qui risqueraient au-delà d'une température de 120°C une altération des huiles de lubrification et la formation d'un mélange détonant.
- Corrosion des métaux, joints et lubrifiants : Attaque le cuivre et tous ses alliages. C'est la raison pour laquelle les installations frigorifiques fonctionnant à l'ammoniac sont réalisées avec des tuyauteries en acier.
- Miscibilité et solubilité : Très soluble dans l'eau et non miscible avec les huiles naphténiques et les huiles de synthèse. Lorsqu'il est dissous dans l'eau, le gaz ammoniac forme une base, l'ammoniaque, de formule NH4OH. L'ion ammonium NH4+ comporte dans ce cas un atome d'hydrogène aux quatre sommets du tétraèdre.
Production industrielle
La production industrielle de l'ammoniac se fait principalement par synthèse directe à partir de dihydrogène et de diazote (procédé mis au point par l'Allemand Fritz Haber, prix Nobel de chimie en 1918). L'azote est apporté par l'air et le dihydrogène par vaporéformage du méthane (gaz naturel).
- méthane + air (source de diazote) + eau → ammoniac + dioxyde de carbone
Qui peut se décomposer en :
- Production de dihydrogène par vaporéformage (voir l'article dihydrogène) :
- Synthèse de l'ammoniac
Ancienne méthode de fabrication
Anciennement, l'ammoniac était obtenu par distillation du purin et du fumier. Au début du XXè siècle différents procédés de synthèse ont été imaginés. L'un d'entre eux se base sur l'hydrolyse de la cyanamide calcique elle même obtenue à partir du carbure de calcium.
L'autre utilise l'hydrolyse du nitrure d'aluminium lui même produit par nitruration à haute température de l'alumine.
Il faut attendre 1910 pour voir apparaître le procédé Haber Bosch encore employé actuellement.
Phrases de risque et conseils de prudence selon l'INRS
R10 – Inflammable.
R23 – Toxique par inhalation.
R34 – Provoque des brûlures.
R50 – Très toxique pour les organismes aquatiques.
S9 – Conserver le récipient dans un lieu bien ventilé.
S16 – Conserver à l'écart de toute flamme ou source d'étincelle. Ne pas fumer.
S26 – En cas de contact avec les yeux laver immédiatement et abondamment avec de l'eau et consulter un spécialiste.
S36/37/39 – Porter un vêtement de protection approprié, des gants et un appareil de protection des yeux/du visage.
S45 – En cas d'accident ou de malaise, consulter immédiatement un médecin (si possible lui montrer l'étiquette).
S61 – Éviter le rejet dans l'environnement. Consulter les instructions spéciales / la fiche de données de sécurité.
Liens sécurité
Référence ONU pour le transport des matières dangereuses
- Classe 2
- numéros :
- 1005 (ammoniac anhydride)
- 3318 (ammoniac en solution aqueuse de densité inférieure à 0,880 à 15 °C contenant plus de 50 % d'ammoniac)
- 2073 (ammoniac en solution aqueuse de densité inférieure à 0,880 à 15 °C contenant plus de 35 % mais au maximum 50 % d'ammoniac)
- numéros :
- Classe 8
- numéro 2672 (ammoniac en solution aqueuse de densité comprise entre 0,880 et 0,957 à 15 °C contenant plus de 10 % mais au maximum 35 % d'ammoniac)
Utilisation
Sous forme gazeuse, l'ammoniac est utilisé par l'industrie pour la fabrication d'engrais, d'explosifs et de polymères. L'ammoniac gazeux, qui donne 82 % d'azote, sert aussi d'engrais azoté ; il est injecté directement dans le sol sous forme d'ammoniac liquéfié sous pression. On le trouve aussi dans la cigarette.
Réfrigération
En tant que fluide frigorigène, l'ammoniac est désigné par la référence R717.
- La lettre R veut dire réfrigérant.
- 7 : les fluides frigorigènes d'origine inorganique sont répertoriés dans la série des 700. Le chiffre des centaines est par conséquent un 7
- 17 : le chiffre des dizaines et celui des unités ici représentent la masse molaire de la molécule à savoir M (NH3) =17,0g. mol-1. En effet la masse molaire atomique de l'azote est M=14,0g. mol-1 et celle de l'hydrogène M=1,0g. mol-1, ce qui nous donne 14,0+3,0=17,0.
Détection des fuites
Du fait de son odeur spécifique, une fuite d'ammoniac est aisément identifiable à l'odorat. Techniquement, on utilise une baguette soufrée, qui enflammée au voisinage d'émanation d'ammoniac produit une fumée blanche dense autorisant ainsi de localiser l'origine de la fuite. La recherche de fuite sur une installation ammoniac ne peut se faire qu'a l'aide d'un ARI (appareil respiratoire individuel) du fait de sa très forte toxicité.
Notes et références
Voir aussi
Recherche sur Google Images : |
|
"DéTECTEUR DE L'AMMONIAC MWG 011 RC ..." L'image ci-contre est extraite du site www.edgb2b.com Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (405 x 320 - 15 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : Refaire la recherche Refaire la recherche |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 12/11/2008.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.




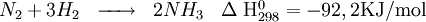
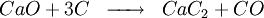
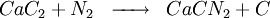
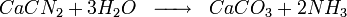
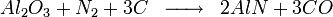
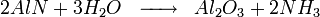



 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité